Spis treści
- Spastyczność: Kompletny Przewodnik dla Pacjentów i Opiekunów
- Czym jest spastyczność?
- Główne przyczyny spastyczności
- Objawy spastyczności
- Diagnostyka spastyczności
- Metody farmakologiczne leczenia spastyczności
- Neurochirurgiczne i interwencyjne metody leczenia
- Metody rehabilitacyjne i fizjoterapii
- Pozycjonowanie i zmniejszenie spastyczności
- Zaopatrzenie ortopedyczne i pomocnicze
- Aspekty społeczne i psychologiczne
- Jak samodzielnie zarządzać spastycznością w domu
- Podsumowanie
Spastyczność: Kompletny Przewodnik dla Pacjentów i Opiekunów
Spastyczność to wzmożone napięcie mięśniowe, które znacząco wpływa na zdolności ruchowe i jakość życia. Artykuł ten wyjaśnia przyczyny spastyczności, dostępne metody leczenia, strategie rehabilitacji oraz wsparcie socjalne dla pacjentów i ich opiekunów w Polsce.
Czym jest spastyczność?
Spastyczność to wzmożone napięcie mięśniowe zależne od prędkości ruchu (velocity-dependent hypertonicity), charakteryzujące się wzmożonym oporarem mięśni podczas pasywnego rozciągania. Napięcie to jest wynikiem zaburzenia funkcji górnego neuronu ruchowego i stanowi objaw zespołu górnego neuronu ruchowego (UMNL).
Różnica między spastycznością a normalnością mieści się w odpowiedzi nerwowo-mięśniowej. Podczas ruchu pasywnego (wykonanego przez drugą osobę) mięśnie pacjenta ze spastycznością wykazują opór, który początkowo może być nieznaczny, ale szybko rośnie wraz ze wzrostem prędkości rozciągania. Zjawisko to stanowi podstawę diagnostyczną i rozróżnia spastyczność od zwykłej sztywności mięśniowej.
Spastyczność rozwija się w wyniku uszkodzenia lub dysfunkcji ośrodkowego układu nerwowego (mózgu lub rdzenia kręgowego). Zdrowy układ nerwowy reguluje mięśnie poprzez sygnały hamujące wysyłane z mózgu. Gdy te sygnały zaburzają się, rezultatem jest wzmożone napięcie mięśniowe.
Zjawisko spastyczności jest częste i dotyczy milionów ludzi na świecie. W Polsce szacuje się, że spastyczność dotyka co najmniej kilkadziesiąt tysięcy osób, zwłaszcza wśród pacjentów po udarze mózgu, z mózgowym porażeniem dziecięcym lub ze stwardnieniem rozsianym.
Główne przyczyny spastyczności
Spastyczność wynika z dysfunkcji ośrodkowego układu nerwowego i może być spowodowana różnymi stanami neurologicznymi. Poniższe warunki to najczęstsze przyczyny spastyczności w praktyce klinicznej:
Udar mózgu (najczęstsza przyczyna u dorosłych)
Udar mózgu to najczęstsza przyczyna spastyczności u dorosłych, zwłaszcza u osób powyżej 65 roku życia. Udar mózgu następuje, gdy przepływ krwi do mózgu zostaje nagłe przerwany, niszcząc komórki mózgowe w zaopatrzywanym obszarze.
Spastyczność po udarze mózgu może się pojawić w ciągu kilku dni do kilku tygodni od momentu udaru. Pacjenci zwykle doświadczają wzmożonego napięcia mięśniowego po stronie ciała przeciwnej do uszkodzonego półkula mózgu. Na przykład udar lewej półkuli mózgu powoduje spastyczność prawej strony ciała.
Około 30% do 40% pacjentów po udarze mózgu rozwija spastyczność w ciągu pierwszych 3 do 6 miesięcy od incydentu. Wczesne rozpoznanie i interwencja rehabilitacyjna istotnie poprawiają wyniki leczenia i funkcjonalność pacjenta.
Jakość rehabilitacji w pierwszych tygodniach po udarze jest krytyczna. Pacjenci, którzy otrzymują wczesną intensywną fizjoterapię, osiągają lepsze rezultaty niż ci, których rehabilitacja jest opóźniona lub mniej intensywna.
Mózgowe porażenie dziecięce (MPD/cerebral palsy)
Mózgowe porażenie dziecięce jest najczęstszą przyczyną spastyczności u dzieci. MPD to grupa trwałych zaburzeń rozwojowych wynikających z uszkodzenia mózgu przed, podczas lub w ciągu 28 dni po urodzeniu.
Spastyczne MPD stanowi około 80% wszystkich przypadków mózgowego porażenia dziecięcego. Dzieci z tym typem MPD wykazują charakterystyczne wzmożone napięcie mięśniowe, problemy z koordynacją ruchową i utrudnioną kontrolę ruchu.
Przyczyny MPD obejmują: wcześniactwo, niską masę urodzeniową, infekcje prenatalne (takie jak toksoplazmooza lub różyczka), niedotlenienie podczas porodu, żółtaczkę noworodków, urazy durante porodu oraz defekty genetyczne. Wiele przypadków MPD jest zabezpieczane poprzez opiekę prenatalno-porodową, ale około 10% do 15% przypadków wynika z czynników przyrodniczych nie dających się zapobiec.
Wczesna diagnoza i interwencja są kluczowe dla optymalnego rozwoju dziecka. Dzieci, które otrzymują wczesne wspomaganie rozwoju (WWR) już w pierwszym roku życia, wykazują lepsze perspektywy funkcjonalne.
Stwardnienie rozsiane (SM)
Stwardnienie rozsiane to choroba autoimmunologiczna, w której system immunologiczny atakuje mielinę – otoczkę chroniącą włókna nerwowe. Spastyczność w SM wynika z demielinizacji i zapalenia w mózgu i rdzeniu kręgowym.
Spastyczność w stwardnieniu rozsianym dotyczy około 60% do 84% pacjentów z SM w pewnym momencie ich choroby. Spastyczność może być stopniowa lub pojawiać się nagłe i może się pogorszyć podczas zaostrzeń choroby.
Pacjenci z SM często doświadczają współwystępującej zmęczenia neurologicznego, problemów ze wzrokiem, zaburzeń kontroli pęcherza moczowego i zaburzeń kognitywnych. Spastyczność w SM wymaga kompleksowego leczenia obejmującego modificiające przebieg choroby terapie (DMT), farmakoterapię antyspastyczną i intensywną rehabilitację.
Prognoza pacjentów z SM znacznie się poprawiła w ostatnich 20 latach dzięki wprowadzeniu nowoczesnych leków modyfikujących przebieg choroby. Jednak spastyczność pozostaje jednym z najbardziej niepokojących objawów dla wielu pacjentów.
Uraz rdzenia kręgowego (SCI)
Uraz rdzenia kręgowego powoduje przerwanie połączeń nerwowych między mózgiem a resztą ciała. Spastyczność jest bardzo częstym powikłaniem urazu rdzenia, rozwijając się w ciągu kilku tygodni do miesięcy po urazie.
Około 65% do 78% osób z urazem rdzenia kręgowego doświadcza spastyczności. Spastyczność w SCI może być tak nasilona, że zabuża ruchliwość stawów, uniemożliwia wykonywanie czynności dnia codziennego i pogorszeniu bólu neuropatycznego.
Pacjenci z parapleją (porażeniem obu nóg) lub tetrapleją (porażeniem wszystkich czterech kończyn) mogą mieć różne stopnie spastyczności. Wczesna, agresywna rehabilitacja i farmakoterapia antyspastyczna mogą zmniejszyć nasilenie spastyczności i poprawić funkcjonalność.
Spastyczność w SCI może również pełnić pewną rolę funkcjonalną – może pomagać pacjentom w stanięciu lub chodzeniu z pomocą. Jednak jeśli spastyczność staje się zbyt nasilona, stanowi główną przeszkodę dla niepełnosprawności.
Stwardnienie zanikowe boczne (ALS)
Stwardnienie zanikowe boczne jest śmiertelną chorobą neuronu ruchowego, która prowadzi do postępującego osłabienia mięśni. Spastyczność w ALS wynika z dysfunkcji górnych neuronów ruchowych, które sterują dolnymi neuronami ruchowymi.
Spastyczność w ALS może powodować sztywność i drażliwość mięśni, co utrudnia ruchy pacjenta. Około 40% do 60% pacjentów z ALS doświadcza spastyczności w pewnym momencie choroby.
Spastyczność w ALS wymaga zarządzania farmakologicznego, zwykle przy użyciu baklofen, tizanidyny lub benzodiazepiny. Pacjenci z ALS należą do grupy wymagającej specjalistycznej opieki, ponieważ choroba szybko się postępuje.
Uraz czaszkowo-mózgowy (TBI)
Uraz czaszkowo-mózgowy to uszkodzenie mózgu spowodowane urazem głowy. Spastyczność jest częstym powikłaniem poważnych TBI, rozwijającym się w ciągu dni do tygodni po urazie.
Pacjenci z TBI mogą wykazywać spastyczność w kombinacji z innymi objawami neurologicznymi, takimi jak zaburzenia poznawcze, problemy z równowagą i zaburzenia zachowania. Nasilenie spastyczności w TBI zależy od lokalizacji i rozmiaru uszkodzenia mózgu.
Rehabilitacja pacjentów z TBI jest kompleksowa i wymaga podejścia wielodyscyplinarnego obejmującego fizjoterapię, terapię zajęciową, logopedię i wsparcze psychologiczne.
Objawy spastyczności
Objawy spastyczności mogą być zmienne i zależy od tego, które mięśnie są dotknięte chorobą. Poniższe znaki mogą wskazywać na obecność spastyczności:
Wzmożone napięcie mięśniowe
Wzmożone napięcie mięśniowe to główny objaw spastyczności, polegający na sztywności i oporze mięśni podczas pasywnego rozciągania. Pacjenci lub opiekunowie mogą zauważyć, że poruszanie ręką lub nogą pacjenta jest trudne i wymaga siły.
Napięcie może być stałe lub pojawiać się okresowo. Może się pogorszyć po stresie, zmęczeniu lub zmianie temperatury otoczenia. Pacjenci sami mogą opisać, że ich mięśnie czują się "napięte" lub "sztywne".
Zmniejszona ruchliwość stawów
Zmniejszona ruchliwość stawów wynika z przewlekłego wzmożonego napięcia mięśniowego. Gdy spastyczność jest niewystarczająco leczona przez długi czas, mięśnie kurczą się trwale (przykurcze), uniemożliwiając pełny zakres ruchu.
Pacjenci mogą mieć trudności z rozciągnięciem ręki lub nogi do pełnego zakresu. W ciężkich przypadkach stawy mogą być zafiksowane w nieprawidłowym położeniu, powodując zaburzenia funkcjonalne i dyskomfort.
Niezgrabne ruchy
Niezgrabne ruchy są wynikiem zaburzonej kontroli ruchowej. Pacjenci mogą wykonywać ruchy powolne, chwiejne lub nieskontrolowane. U dzieci z MPD ruchy mogą być niekoordynacyjne i asymetryczne.
Pacjenci mogą mieć trudności z precyzyjnym wykonywaniem czynności, takich jak pisanie, jedzenie lub ubieranie się. Niezgrabność może się pogorszyć ze zmęczeniem lub stresem.
Przykurcze mięśniowe
Przykurcze mięśniowe to trwałe skrócenie mięśni wynikające z przewlekłej spastyczności. Przykurcze może prowadzić do trwałych deformacji stawów i znacznie ograniczyć funkcjonalność pacjenta.
Zapobieganie przykurczu jest ważne i wymaga konsekwentnego wykonywania ćwiczeń rozciągających i pozycjonowania. Raz wytworzone przykurcze mogą być trudne do odwrócenia, dlatego profilaktyka jest niezbędna.
Klonus
Klonus to rytmiczne, niekontrolowane skurcze mięśni, zwykle spowodowane gwałtownym rozciągnięciem mięśnia. Klonus może być pobroczny (kilka skurczów) lub trwały (wiele następujących po sobie skurczów).
Klonus jest szczególnie widoczny w stopie lub ręce i może być wyzwalany pasywnym rozciągnięciem mięśnia. Klonus nie jest bolesny, ale może być niepokojący dla pacjenta.
Ból i dyskomfort
Ból może towarzyszyć spastyczności i wynikać z wzmożonego napięcia mięśniowego, przykurczów lub skurczów mięśni. Pacjenci mogą doświadczać bólu mięśniowego, stawowego lub neuropatycznego.
Ból może wpływać na jakość snu, nastrój i motywację do rehabilitacji. Zarządzanie bólem jest ważnym elementem leczenia spastyczności.
Diagnostyka spastyczności
Diagnostyka spastyczności opiera się na badaniu klinicznym i ocenie funkcjonalnej. Poniższe narzędzia diagnostyczne są standardowo stosowane:
Skala Ashworth (Modified Ashworth Scale – MAS)
Skala Ashworth jest najczęściej używanym narzędziem do pomiaru nasilenia spastyczności w praktyce klinicznej. Skala ta mierzy opór mięśni podczas pasywnego rozciągania i ocenia nasilenie spastyczności na skali 0-4.
Procedura badania Skalą Ashworth obejmuje powolne, pasywne rozciąganie mięśnia przez kilka sekund i ocenę oporów, które lekarz odczuwa. Skalę tę można zastosować do poszczególnych mięśni lub grup mięśniowych.
Interpretacja wyniku Skali Ashworth:
- 0 = brak wzmożonego napięcia
- 1 = lekkie wzmożenie napięcia wyczuwalne na końcu zakresu ruchu
- 1+ = lekkie wzmożenie napięcia, mniejszy opór przez mniej niż połowę zakresu ruchu
- 2 = bardziej wyraźne wzmożenie napięcia przez większość zakresu ruchu
- 3 = znaczne wzmożenie napięcia, opór pasywny ruchu
- 4 = mięśnie sztywne w zgięciu i wyprostowaniu
Skala Ashworth jest szybka, łatwa w stosowaniu i nie wymaga specjalnego sprzętu. Jest używana zarówno w pierwszej ocenie, jak i do monitorowania zmian spastyczności w trakcie leczenia. Jej ograniczeniem jest subiektywność, dlatego najlepiej, jeśli ten sam badacz ocenia pacjenta w kolejnych wizytach.
Skala Tardieu
Skala Tardieu jest bardziej czułą miarą spastyczności niż Skala Ashworth. Skala Tardieu mierzy zarówno opór mięśni, jak i klonus podczas ruchu pasywnego w określonej prędkości.
Procedura badania Skalą Tardieu obejmuje pasywne rozciągnięcie mięśnia w trzech różnych prędkościach (powolnie, szybko i szybko-szybko) i ocenę oporów przy każdej prędkości. Skala zawiera również ocenę klonusu.
Skala Tardieu jest bardziej złożona niż Skala Ashworth i wymaga szkolenia, aby ją prawidłowo stosować. Jednak jej wyższa czułość czyni ją użyteczną do monitorowania subtelnych zmian spastyczności, zwłaszcza u dzieci z MPD.
Elektromiografia (EMG)
Elektromiografia to test, który mierzy aktywność elektryczną mięśni. W spastyczności EMG może wykazać zwiększoną aktywność elektryczną mięśni nawet w stanie spoczynku, co wskazuje na wzmożone napięcie.
EMG jest używana głównie do diagnostyki warunków pierwotnych (takich jak neuropatia lub miopatia), które mogą przedszedzać spastyczność. W praktyce klinicznej EMG rzadko jest konieczna do diagnozy spastyczności, ale może być przydatna w skomplikowanych przypadkach.
Rezonans magnetyczny (MRI) mózgu i rdzenia kręgowego
Rezonans magnetyczny jest używany do identyfikacji przyczyny spastyczności. MRI może pokazać obszary uszkodzenia mózgu (po udarze), demielinizację (w SM), urazy rdzenia kręgowego lub inne zaburzenia neurologiczne.
MRI nie jest konieczny do diagnozy samej spastyczności, ale jest ważny do ustalenia przyczyny i planowania leczenia. MRI jest szczególnie ważny u pacjentów z nowo rozpoznaną spastycznością bez jasnej przyczyny.
Badanie neurologiczne
Badanie neurologiczne przeprowadzane przez lekarza neurologa lub specjalistę rehabilitacji jest kluczowe do oceny spastyczności. Badanie to obejmuje:
Badanie neurologiczne funkcjonalne pozwala ocenić wpływ spastyczności na zdolności funkcjonalne pacjenta. Badanie obejmuje obserwację, jak pacjent porusza się, stoi, chodzi (jeśli jest to możliwe) i wykonuje codzienne czynności.
Metody farmakologiczne leczenia spastyczności
Leczenie farmakologiczne jest pierwszą linią terapii spastyczności i odgrywa kluczową rolę w zarządzaniu objawami. Poniższe leki są najczęściej stosowane:
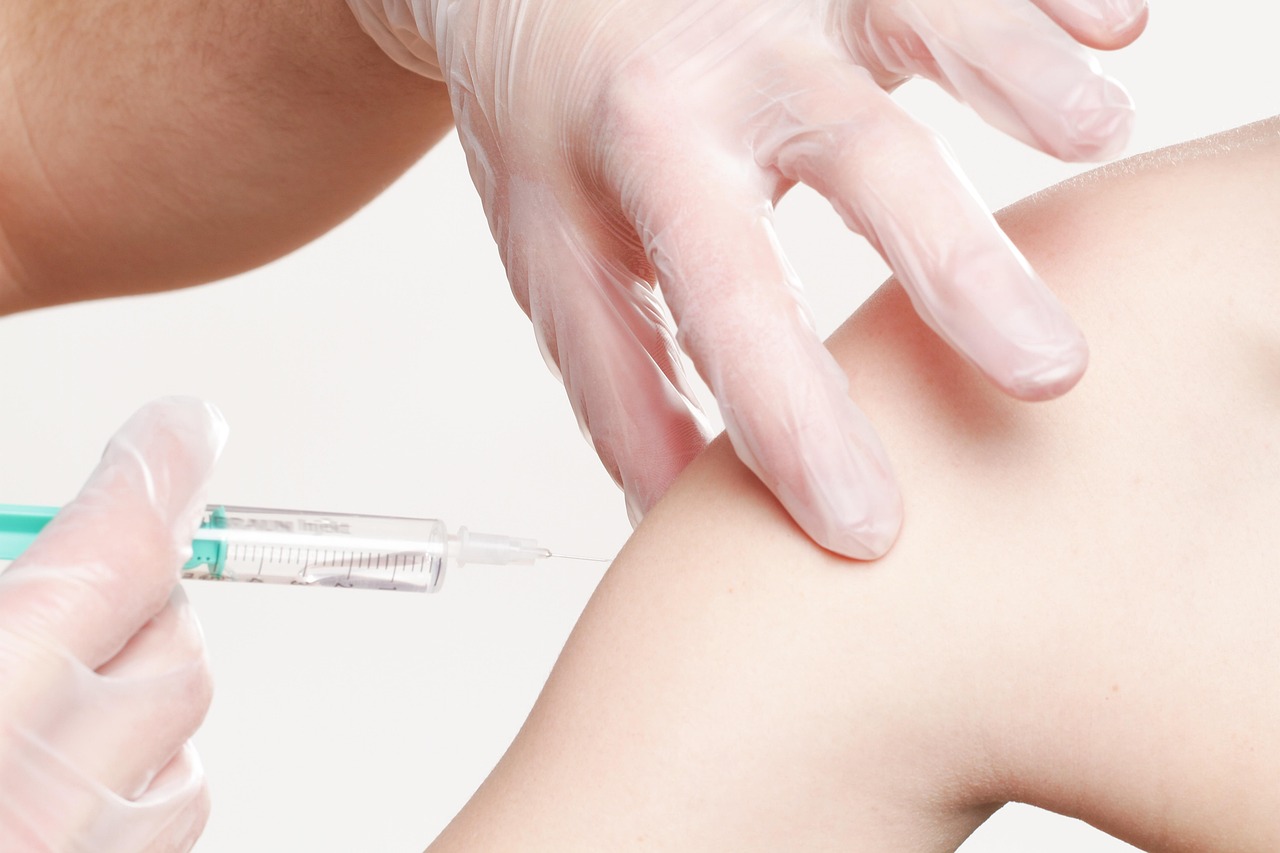
Toksyna botulinowa (Botox, Dysport, Xeomin)
Toksyna botulinowa jest najbardziej selektywnym lekiem do leczenia ogniskowej spastyczności i jest uważana za złoty standard w leczeniu spastyczności ogniskowej. Toksyna botulinowa blokuje uwalnianie acetylocholiny na złączu neuromięśniowym, powodując czasowe osłabienie mięśni.
Procedura wstrzyknięcia toksyny botulinowej obejmuje dokładną identyfikację hipertonicznych mięśni, często z pomocą ultrasonu lub elektromiografii. Lekarz wstrzykuje tokszynę botulinową bezpośrednio do mięśnia, a efekt następuje w ciągu 3 do 7 dni, osiągając maksimum w ciągu 2 do 4 tygodni.
Trzy główne preparaty toksyny botulinowej dostępne w Polsce:
Botox (onabotulinum toksin A) – oryginalny preparat i najdłużej stosowany w praktyce klinicznej. Botox jest dostępny w strengach 50 i 100 jednostek i jest refundowany przez NFZ do leczenia spastyczności. Efekt Botoxu trwa średnio 3 do 4 miesiące.
Dysport (abobotulin toksin A) – preparat z potencjalnie szybszym rozproszeniem niż Botox. Dysport jest również refundowany przez NFZ i trwa średnio 3 do 4 miesiące. Dysport może być bardziej odpowiedni dla pacjentów, u których Botox jest niewystareczny.
Xeomin (incobotulin toksin A) – najnowszy preparat bez białek pomocniczych. Xeomin jest mniej immunogeniczny niż Botox i Dysport. Xeomin jest dostępny w Polsce, ale nie jest refundowany przez NFZ dla spastyczności, dlatego znacznie droższy niż Botox i Dysport.
Wskazania do wstrzyknięcia toksyny botulinowej obejmują spastyczność ogniskową w konkretnych mięśniach lub grupach mięśniowych (takie jak napięcie dziecka w stawach zgiętych kończyn górnych w MPD) oraz spastyczność, która nie reaguje odpowiednio na leki doustne. Pacjenci powinni być ocenieni przez specjalistę, aby określić, czy są kandydatami do leczenia toksynie botulinową.
Przeciwwskazania do wstrzyknięcia toksyny botulinowej obejmują: infekcję w miejscu wstrzyknięcia, alergię na którąkolwiek składnik preparatu, ciążę i karmienie piersią. Pacjenci ze zdyagnozowanymi zaburzeniami neuromięśniowymi (takimi jak miastenia gravis) mogą być wrażliwi na tokszynę botulinową i wymagają szczególnej ostrożności.
Efekty uboczne toksyny botulinowej są zwykle przejściowe i mniej powszechne niż efekty uboczne leków doustnych. Możliwe efekty uboczne obejmują: ból, zaczerwienienie i obrzęk w miejscu wstrzyknięcia, osłabienie pobliskich mięśni, czasem słabość, która jest niezamierzona. Ciężkie efekty uboczne (takie jak rozprzestrzenianie się toksynu poza miejsce wstrzyknięcia) są niezwykle rzadkie.
Koszty toksyny botulinowej w Polsce są zróżnicowane. Refundacja NFZ wynosi zazwyczaj około 1500-2000 złotych za zabiegi, jednak mogą być dni oczekiwania na refundację. Pacjenci mogą również wybrać leczenie prywatne, które kosztuje zwykle 2000-3500 złotych za zabiegi.
Baklofen (doustny i dokanałowy/pompa baklofenowa ITB)
Baklofen jest najpowszechniej stosowanym lekiem doustnym do leczenia spastyczności i jest pierwszym wyborem leku dla większości pacjentów. Baklofen działa poprzez agonizm receptorów GABA-B, zmniejszając pobudzenie neuronów.
Dawkowanie baklofen doustny rozpoczyna się zwykle od 5 mg trzy razy dziennie i jest stopniowo zwiększane co kilka dni do skutecznej dawki, zwykle w zakresie 30-80 mg dziennie w podziale na 3-4 dawki. Maksymalna zalecaną dawka wynosi 80 mg dziennie, jednak niektórzy pacjenci mogą wymagać wyższych dawek.
Efekt baklofen zostaje zaobserwowany w ciągu 3 do 7 dni po jego rozpoczęciu, a pełny efekt może być osiągnięty dopiero po kilku tygodniach. Dlatego pacjenci muszą wykazać cierpliwość podczas titracjii dawki.
Baklofen doustny jest dobrze tolerowany przez większość pacjentów, ale może mieć efekty uboczne, zwłaszcza we wczesnych stadiach leczenia. Możliwe efekty uboczne obejmują: słabość, zmęczenie, zawroty głowy, bezsenność, nudności i zaparcia. Większość efektów ubocznych zmniejsza się lub znika w ciągu kilku dni do tygodni.
Ograniczenie baklofen doustny jest jego działaniem systemowym – lek wpływa na cały układ nerwowy, co prowadzi do uogólnionej słabości i zmęczenia. Ponadto, baclofen nie może być nagłe przerwany, ponieważ nagłe zaprzestanie może spowodować zespół wymiany z objawami takimi jak zawroty głowy, bezsenność, drażliwość i w ciężkich przypadkach zawały.
Pompa baklofenowa (intratekalna dostawa baklofen – ITB)
Pompa baklofenowa jest urządzeniem implantowanym chirurgicznie, które dostarcza baklofen bezpośrednio do płynu mózgowo-rdzeniowego. Pompa baklofenowa pozwala na znacznie mniejsze dawki baklofen (zazwyczaj 300-800 µg dziennie) w porównaniu z baklofen doustny (30-80 mg dziennie).
Wskazania do zabiegu implantacji pompy baklofenowej obejmują: poważna spastyczność, która nie reaguje odpowiednio na baklofen doustny lub inne leki; pacjenci, którzy nie tolerują efektów ubocznych baklofen doustny; pacjenci z przewlekłą spastycznością, dla których inne metody są niewystarczające.
Procedura implantacji pompy baklofenowej jest chirurgiczna i wymaga: 1) implantacji gęstej kateterze do kanału rdzeniowego; 2) implantacji zasobnika leku pod skórę pacjenta; 3) programowania pompy za pomocą zewnętrznego urządzenia programującego.
Po implantacji pacjent wymaga regularnych wizyt w ośrodku specjalizowanym (zwykle co 4-12 tygodni) do napełniania zbiornika baklofen i weryfikacji ustawień pompy. Koszty pompy baklofenowej w Polsce mogą być wysokie, ale pacjenci mogą kwalifikować się do refundacji NFZ pod pewnymi warunkami.
Zaletą pompy baklofenowej jest znacznie wyższe działanie (mniejsze dawki) i mniejsze efekty uboczne niż baklofen doustny. Jednak procedura jest chirurgiczna i wiąże się z ryzykiem powikłań (takich jak infekcja, nieszczelność kateterze, upadek zbiornika).
Tizanidyna (Sirdalud)
Tizanidyna jest lekiem alfą-2-adrenergicznym agonistą, który działa poprzez wzmacnianie presynaptycznego hamowania. Tizanidyna zmniejsza glutamat i substancję P, które są excytacyjnymi neurotransmiterami zaangażowanymi w spastyczność.
Dawkowanie tizanidyna rozpoczyna się zwykle od 2 mg jeden raz dziennie i jest powoli zwiększane co kilka dni do skutecznej dawki, zwykle w zakresie 6-12 mg dziennie w podziale na 3 dawki. Maksymalna zalecaną dawka wynosi 36 mg dziennie.
Tizanidyna jest szybciej działająca niż baklofen (efekt w ciągu 1-2 godzin) i może być wygodniej dla pacjentów, którzy potrzebują szybkiego ulgi. Tizanidyna jest szczególnie użyteczna w przypadkach spastyczności z towarzysztacym bólem.
Efekty uboczne tizanidyna obejmują: suche usta, zawroty głowy, zmęczenie, nudności i zaburzenia czynności wątroby (zwłaszcza w wyższych dawkach). Tizanidyna wymaga monitorowania czynności wątroby poprzez regularne badania krwi.
Ponieważ tizanidyna jest metabolizowana w wątrobie, pacjenci z zaburzeniami funkcji wątroby mogą wymagać mniejszych dawek. Tizanidyna może również wchodzić w interakcje z innymi lekami metabolizowanymi przez wątrobę.
Dantrolen (Dantrium)
Dantrolen jest lekiem, który działa obwodowo poprzez hamowanie uwalniania wapnia ze zbiornika wewnątrzkomórkowego w mięśniach. Dantrolen jest działaniem bardziej bezpośrednim na mięśnie niż baclofen lub tizanidyna.
Dantrolen jest mniej powszechnie stosowany niż baclofen lub tizanidyna z powodu wyższego ryzyka hepatotoksyczności (uszkodzenia wątroby) i konieczności regularnego monitorowania funkcji wątroby. Dantrolen jest rezerwowany dla pacjentów, którzy nie tolerują lub nie odpowiadają na inne leki antyspastyczne.
Dawkowanie dantrolen rozpoczyna się od 25 mg jeden raz dziennie i jest zwiększane co kilka dni do maksymalnej dawki 400 mg dziennie w podziale na 4 dawki. Jednak większość pacjentów toleruje maksimum 200-300 mg dziennie z powodu efektów ubocznych.
Benzodiazepiny (diazepam, klonazepam)
Benzodiazepiny, zwłaszcza diazepam, są stosowane do zmniejszenia spastyczności i skojarzeń mięśniowych. Benzodiazepiny działają poprzez wzmacnianie hamowania GABA w mózgu i rdzeniu kręgowym.
Diazepam jest zwykle dawkowany w dawkach 2-10 mg jeden raz dziennie lub podzielony na kilka dawek. Klonazepam może być dawkowany w dawkach 0,5-2 mg dziennie.
Benzodiazepiny są przydatne do doraźnego zmniejszenia spastyczności, ale nie są zalecane dla długotrwałego stosowania z powodu ryzyka zależności i tolerancji. Efekty uboczne benzodiazepiny obejmują: sedację, zawroty głowy, zmęczenie, zaburzenia pamięci i zaburzenia koordynacji.
Gromadzenie benzodiazepiny powoduje skumulowanie się leku w organizmie, zwiększając ryzyko efektów ubocznych. Benzodiazepiny powinny być używane ostrożnie u pacjentów starszych i tych z zaburzeniami oddechu.
Neurochirurgiczne i interwencyjne metody leczenia
Gdy farmakoterapia jest niewystareczna, pacjenci mogą kwalifikować się do procedur neurochirurgicznych lub interwencyjnych:
Rizotomia selektywna dorsalna (SDR)
Rizotomia selektywna dorsalna to procedura chirurgiczna, w której chirurg przecina pierwiastkami dorzednymi (pierwiastkami czuciowymi) w rdzeniu kręgowym, aby zmniejszyć spastyczność. Rizotomia selektywna dorsalna jest szczególnie wskazana u dzieci z MPD i innych pacjentów z poważną spastycznością dolnych kończyn.
Procedura rizotomia selektywna dorsalna obejmuje: 1) otwarcie rdzenia kręgowego w okolicy L3-L5; 2) identyfikację pierwiastkami dorsalnych (czuciowych); 3) wyboru pierwszych pierwiastków przy użyciu stymulacji elektrycznej (pierwiastkami, które wykazują opory przy stymulacji) i przecięcia ich; 4) przywrócenia normalnych pierwszych pierwiastków.
Efekt rizotomia selektywna dorsalna na zmniejszenie spastyczności jest znaczący i może być trwały. Jednak procedura jest chirurgiczna z ryzykiem powikłań takich jak: infekcja, torbiele postrizotomijne (rzadko), zaburzenia czucia (zwłaszcza w stopie) i zaburzenia kontroli pęcherza moczowego.
Wskazania do SDR obejmują pacjentów z MLFczą klinicznych kryteriów: poważna spastyczność (MAS 3-4); pacjenci są poniżej 80 lat; brak poważnych zaburzeń poznawczych; spastyczność głównie w dolnych kończyn; brak poważnych deformacji lub przykurczów.
Wyniki SDR są zróżnicowane. Około 80-90% pacjentów doświadcza zmniejszenia spastyczności o 50% lub więcej. Jednak pacjenci mogą również doświadczać zaburzeń czucia w stopach, zmęczenia czy zaburzeń miąższu.
Fenolizacja i neuroliza
Fenolizacja i neuroliza są procedurami interwencyjnymi, w których alkohol lub fenol jest wstrzyknięty do nerwy, aby zablokować transmisję nerwową i zmniejszyć spastyczność. Te procedury są mniej inwazyjne niż rizotomia, ale efekt jest przejściowy (trwa od kilku tygodni do kilku miesięcy).
Fenolizacja może być stosowana do nerwów obwodowych (np. nerw posłankowy, nerw piszczelowy) i jest szczególnie użyteczna w spastyczności ogniskowej. Procedura jest często wykonywana pod kontrolą ultrasonu w celu dokładnego umieszczenia igły w nerwie.
Zaletą fenolizacji jest niszczący efekt na nerwy, który trwa dłużej niż toksyna botulinowa (kilka do kilkunastu tygodni). Jednak fenolizacja może powodować ból neuropatyczny jako efekt uboczny.
Metody rehabilitacyjne i fizjoterapii
Rehabilitacja jest kluczowa w zarządzaniu spastycznością i powinna być traktowana jako równoległa do farmakoterapii. Poniższe metody terapeutyczne są stosowane w Polsce:
Fizjoterapia neurologiczna
Fizjoterapia neurologiczna to ogólna kategoria terapii ruchowej stosowanej do pacjentów ze spastycznością i innymi zaburzeniami neurologicznymi. Fizjoterapia neurologiczna obejmuje ćwiczenia wzmacniające, rozciągające, równoważące i funkcjonalne.
Cele fizjoterapii neurologicznej w spastyczności to: zmniejszenie napięcia mięśniowego; utrzymanie i rozszerzenie zakresu ruchu; wzmocnienie oslabioych mięśni; ulepszenie równowagi i koordynacji; osiągnięcie maksymalnej funkcjonalności.
Sesje fizjoterapii powinny być intensywne (najlepiej 3-5 razy na tygodniu dla pacjentów ambulatoryjnych i codzienna dla pacjentów szpitalnych) i mogą być długie (30-60 minut na sesję). Konsystencja i długotrwałość fizjoterapii są niezbędne do osiągnięcia wyników.
Fizjoterapia jest szczególnie ważna w pierwszych tygodniach i miesiącach po udaru lub innym zaburzeniu neurologicznym, kiedy mózg jest w fazie neuroplastyczności. Jednak nawet pacjenci z przewlekłą spastycznością mogą skorzystać z fizjoterapii, która powinna być dostosowana do ich poziomu funkcjonalności.
Metoda NDT-Bobath
Metoda NDT-Bobath (Neurodevelopmental Treatment) jest wiodącą metodą fizjoterapii w spastyczności, szczególnie u dzieci z MPD i pacjentów po udarze. Metoda NDT-Bobath opiera się na zrozumieniu neuroplastyczności i zdolności mózgu do reorganizacji funkcji.
Principia metody NDT-Bobath obejmuje:
- Inhibicja patologicznych wzorców – terapeuta pracuje na zmniejszeniu anomalnych odruchów i wzorców mięśniowych
- Aktywacja normalnych ruchów – pacjent uczy się prawidłowych wzorów ruchu poprzez praktykę i powtórzenie
- Funkcjonalny trening – ćwiczenia są zorientowane na codzienne czynności
- Indywidualizacja – program jest dopasowywany do potrzeb i zdolności danego pacjenta
W praktyce terapeuta NDT-Bobath manualne zajmuje się pacjentem, korygując pozycję ciała, ułatwiając prawidłowe ruchy i zmniejszając napięcie mięśniowe poprzez właściwe ułożenie i pointa hnięcia (key points of control).
Metoda NDT-Bobath wymaga znacznych umiejętności i doświadczenia od terapeuty, ponieważ każdy pacjent wymaga innego podejścia. Terapeuta musi obserwować pacjenta, identyfikować patologiczne wzorce i dostosowywać techniki w rzeczywistym czasie.
Wyniki metody NDT-Bobath są dobrze udokumentowane w literaturze naukowej. Pacjenci poddani NDT-Bobath wykazują znacznie lepsze wyniki funkcjonalne niż pacjenci, którzy otrzymują ogólną fizjoterapię.
Metoda Vojty
Metoda Vojty (tzw. terapia odruchowej lokomocji) opiera się na założeniu, że mózg zawiera wbudowane programy ruchów dziecka do poruszania się (pełzania i chodzenia). Metoda Vojty aktywuje te programy poprzez stymulację określonych punktów na ciele pacjenta.
Terapeuta Vojty używa specyficznych chwytów manualnych w określonych punktach aktywacyjnych (zwłaszcza w obrębie żeber i miednicy) dla wyzwolenia specyficznych odruchowych ruchów lokomocji. Pacjent zobowiązany jest do wykonania tych ruchów powtarzalnie.
Metoda Vojta jest szczególnie popularna w Niemczech i Polsce oraz jest częścią standardowego leczenia MPD u dzieci. Metoda wymaga konsekwentnego treningu (zwykle 3-4 sesje dziennie po 10-15 minut).
Wyniki metody Vojty są zróżnicowane. Niektórzy pacjenci, zwłaszcza ci z mniej obrażoną funkcją motoryczną, wykazują znaczną poprawę. Jednak pacjenci z ciężką uszkodzeniem (taka jak tetraplastyka dystonie) mogą wykazać mniejszą odpowiedź.
Metoda Vojty jest pracochłonna dla rodziców i opiekunów, którzy muszą wykonywać ćwiczenia codziennie. Jednak siła metody Vojty jest jej możliwością terapeutycznego wpływu na bardzo małych dzieci.
Metoda PNF (proprioceptywne torowanie nerwowo-mięśniowe)
Metoda PNF to technika terapii ruchowej, która wykorzystuje opory i stretching, aby zwiększyć siłę i kontrolę mięśni. PNF można stosować zarówno w spastyczności, jak i w osłabieniu mięśniowym.
W kontekście spastyczności, PNF może być stosowana do zmniejszenia patologicznych wzorów i zwiększenia normalnych ruchów. Terapeuta PNF używa technikh hamowania (takie jak contract-relax) do zmniejszenia spastyczności.
PNF jest efektywna, ale wymaga dobrego wylrenowania terapeuty i aktywnej partycypacji pacjenta. PNF może być intensywna i czasem bolesna, dlatego musi być zastosowana ostrożnie u pacjentów z bólem.
Terapia zajęciowa (OT)
Terapia zajęciowa skupia się na zdolności pacjenta do wykonywania codziennych czynności. Terapeuta zajęciowy pracuje z pacjentem na ulepszeniu funkcjonalności w wykonywaniu czynności takie jak jedzenie, ubieranie się, higiena osobista i czynności domowe.
Terapia zajęciowa jest szczególnie ważna dla pacjentów ze spastycznością w górnych kończynach, gdzie funkcja ręki jest krytyczna dla niezależności. Terapeuta zajęciowy może zalecić adaptacyjne urządzenia i strategie do ułatwienia czynności.
Hydroterapia
Hydroterapia to ćwiczenia wykonywane w wodzie, które są szczególnie przydatne dla pacjentów ze spastycznością. Woda zapewnia wsparcie i zmniejsza efekty grawitacji, co ułatwia ruch.
Ponadto, ciepła woda ma działanie relaksacyjne na mięśnie, zmniejszając spastyczność. Pacjenci mogą wykonywać szerszy zakres ruchu w wodzie niż w lądzie, co pozwala na bardziej funkcjonalne ćwiczenia.
Hydroterapia jest szczególnie skuteczna dla pacjentów, którym zwykła fizjoterapia jest zbyt uciążliwa. Jednak hydroterapia wymaga dostępu do basenu, co jest czasami ograniczą w niektórych ośrodkach.
Robotyka rehabilitacyjna
Robotyka rehabilitacyjna to wykorzystanie robota do ułatwienia ćwiczeń ruchowych. Popularne urządzenia robotyczne w rehabilitacji spastyczności obejmują: Lokomat (do treningu chodzenia), Armeo (do treningu górnych kończyn) i inne roboty.
Robotyka rehabilitacyjna pozwala na powtórzenie dużej liczby ruchów w kontrolowanym środowisku. Roboty mogą również dostarczać biofeedback (informacje zwrotne o wykonaniu ruchu), co motywuje pacjentów.
Badania pokazują, że robot-assisted therapy może być bardziej efektywna niż tradycyjna fizjoterapia w niektórych aspektach (takie jak siła i wytrzymałość), chociaż funkcjonalne wyniki mogą być podobne. Robotyka rehabilitacyjna jest coraz bardzie dostępna w Polsce, ale koszt jest nadal wysoki.
CIMT (Constraint-Induced Movement Therapy)
CIMT to metoda terapii, w której pacjent jest zmuszony do używania słabej ręki poprzez ograniczenie funkcji silnej ręki. CIMT opiera się na założeniu, że mózg wyuczył się ignorować słabszą rękę, a zmuszenie użytkownika zmieniło tę nawykaż.
W CIMT, pacjent ma unieruchomioną lub ograniczoną silną rękę (zwykle za pomocą rękawicy lub temblaka) i wykonuje funkcjonalne zadania słabą ręką przez intensywne sesje (2-3 godziny dziennie przez kilka tygodni).
Badania pokazują, że CIMT jest efektywna w poprawie funkcji ręki po udarze mózgu i innych zaburzeniach neurologicznych. Jednak CIMT jest pracochłonna i wymaga dużej motywacji pacjenta.
Elektrostymulacja funkcjonalna (FES)
Elektrostymulacja funkcjonalna to wykorzystanie elektrycznych prądów do stymulacji mięśni w celu wywoływania skurczów. FES może być stosowana do wzmocnienia osłabioych mieśni i ułatwienia funkcjonalnych ruchów.
FES może być szczególnie przydatna u pacjentów z zupełnym porażenie, gdzie mięśnie nie mogą się skurczyć bez stymulacji. FES może być również użyta do treningów chodzenia (FES-assisted walking) u pacjentów po udarze lub z urazem rdzenia.
Zaletą FES jest możliwość aktywacji mięśni bez wysiłku pacjenta. Jednak FES może być niekomfortowa i wymaga wciągłego noszenia elektrod.
Pozycjonowanie i zmniejszenie spastyczności
Pozycjonowanie jest prostą, ale ważną strategią do zmniejszenia spastyczności i zapobiegania przykurczu. Właściwe pozycjonowanie mięśni w wydłużonym położeniu zmniejsza spastyczność i zapobiega przykurczu.
Znaczenie pozycjonowania
Pozycjonowanie jest szczególnie ważne dla pacjentów z ciężką spastycznością, którzy mają ograniczoną mobilność. Pacjenci, którzy spędzają wiele godzin w jednym położeniu (takie jak siedzenie w wózku inwalidzkim), mogą szybko rozwjąć przykurcze, jeśli mięśnie nie są regularnie rozciągane.
Terapeuta powinna zaapliować pozycjonowanie indywidualnie dla każdego pacjenta, w zależności od tego, które mięśnie są zaangażowane. Na przykład pacjent ze spastyczną połowy nie powinien mieć zgięte ramię przytwierdzone do piersi przez wiele godzin, ponieważ to prowadzi do przykurczów flexorów.
Strategie pozycjonowania
Strategie pozycjonowania obejmują:
- Noční szyny – szynę zmiękczająca na rękę lub nogę na noc, aby utrzymać mięśnie w wydłużonym położeniu
- Dynamiczne szynowanie – szyn, które aplikują łagodne, ciągłe rozciągnięcie mięśni przez kilka godzin dziennie
- Zmiana pozycji – regularna zmiana pozycji podczas dnia (zmiana pozycji sedzenia, leżenia na plecach, leżenia na brzuszu)
- Podpieranie – umieszczanie poduszek pod mięśnie w wydłużonym położeniu
- Podnos nóg – dla pacjentów z edemiąmi nóg, podniesienie nóg zmniejsza obrzęk, co zmniejsza spastyczność
Zaopatrzenie ortopedyczne i pomocnicze
Zaopatrzenie ortopedyczne i pomocnicze jest ważne dla pacjentów ze spastyczością, aby wspierać funkcjonowanie i zapobiegać deformacjom.
Ortezy (AFO, KAFO, WHO)
Ortezy są urządzeniami ortopedycznymi, które wspierają stawy i pomagają w utrzymaniu prawidłowego położenia. Główne typy ortez stosowane w spastyczności to:
AFO (Ankle-Foot Orthosis) – orteza na stopę i kostkę, która utrzymuje stopę w prawidłowym położeniu. AFO jest szczególnie przydatna dla pacjentów ze spastyczną głową stopni (varus foot) po udarze lub w MPD. AFO ułatwia chodzenie i zmniejsza ryzyko upadków.
KAFO (Knee-Ankle-Foot Orthosis) – orteza na kolano, kostkę i stopę. KAFO jest stosowana dla pacjentów z ciężką spastycznością lub słabością dolnych kończyn, którzy potrzebują wsparcia całej nogi.
WHO (Wrist-Hand Orthosis) – orteza na rękę. WHO wspiera przegub ręki i palce, zapobiegając przykurczu flexorów. WHO jest szczególnie przydatna dla pacjentów ze spastycznością górnych kończyn po udarze.
Ortezy mogą być pasywne (nie zawierają części ruchome) lub dynamiczne (zawierają sprężyny lub inne mehanizmy dla dodatkowej mocy). Dynamiczne ortezy mogą być droższe, ale mogą dostarczać więcej wsparcia i motywacji do ruchu.
Ortezy mogą być refundowane przez NFZ, ale pacjent musi spełnić określone kryteria. Pacjenci mogą kwalifikować się do refundacji ortez poprzez: zaświadczenie lekarza neurologa lub rehabilitanta; orzeczenie o niepełnosprawności; złożenie wniosku w ośrodku rehabilitacyjnym.
Szyny statyczne i dynamiczne
Szyny są podobne do ortez, ale zwykle są wykonane z materiałów miększych i mogą być łatwo wkładane i wyjmowane. Szyny statyczne utrzymują mięśnie w wydłużonym położeniu bez dodatkowego siły (zwykle stosowane na noc). Szyny dynamiczne aplikują łagodną, ciągłą siłę, aby powoli rozciągnąć mięśnie (zwykle noszone przez kilka godzin dziennie).
Wózki inwalidzkie
Wózki inwalidzkie są niezbędne dla pacjentów, którzy nie mogą chodzić lub mają trudności w poruszaniu się. Główne typy wózków to:
Wózki ręczne – pacjent napędza wózek ręcznie. Wózki ręczne są lżejsze i bardziej przenośne, ale wymagają siły i koordynacji z rąk pacjenta.
Wózki elektryczne – napędzane baterią. Wózki elektryczne są idealne dla pacjentów, którzy nie mogą samodzielnie napędzać wózka, lub dla tych, które długie distancje.
Wózki aktywne – specjalne wózki zaprojektowane dla pacjentów aktywnych, które pozwalają na dynamiczne pozycjonowanie.
Wybór wózka zależy od poziomu funkcjonalności pacjenta, środowiska, w którym pacjent się porusza (dom, szkoła, miejsca publiczne) i budżetu. Wózki mogą być refundowane przez NFZ lub PFRON pod pewnymi warunkami.
Pionizatory
Pionizatory są urządzeniami, które pomagają pacjentom ze spastycznością w staniu. Pionizatory są szczególnie ważne dla pacjentów, którzy nie mogą stać bez wsparcia (takie jak pacjenci z parapleją po urazem rdzenia).
Stanie ma wiele korzyści: zmniejsza spastyczność, zmniejsza ryzyko osteoporozy, poprawia krążenie krwi, zmniejsza bóle i dyskomfort, oraz poprawia psychiczne samopoczucie pacjenta.
Pionizatory mogą być ręczne (pacjent lub terapeuta napędza) lub elektryczne (automatycznie podnoszą pacjenta). Pionizatory mogą być refundowane przez NFZ pod pewnymi warunkami.
Chodziki i balkoniki
Chodziki i balkoniki zapewniają wsparcie i stabilność dla pacjentów, którzy mogą chodzić, ale mają trudności z równowagą lub są niestabilni. Chodziki mogą zmniejszyć ryzyko upadków i dać pacjentom pewność do poruszania się.
Istnieje wiele typów chodzików: tradycyjne chodziki czteropunktowe, chodziki dwupunktowe (bardziej mobilne), chodziki z kółkami (na podłogach twardych), itp.
Siedziska ortopedyczne
Siedziska ortopedyczne zapewniają wsparcie dla pacjentów w pozycji siedzącej. Prawidłowe siedzisko może zmniejszyć spastyczność, zapobiec deformacjom kręgosłupa i poprawić komfort.
Siedziska ortopedyczne powinny być dostosowane indywidualnie do pacjenta. Terapeuta zajęciowy lub specjalista ortopedyczny może pomóc w wyborze odpowiedniego siedziska.
Aspekty społeczne i psychologiczne
Spastyczność ma znaczący wpływ na jakość życia pacjenta i jego rodziny. Poniższe aspekty powinny być brane pod uwagę w kompleksowym leczeniu:
Orzecznictwo i niepełnosprawność
Pacjenci ze spastycznością mogą kwalifikować się do orzeczenia o niepełnosprawności. Orzeczenie o niepełnosprawności otwiera dostęp do wielu świadczeń i uprawnień.
Rodzaje orzeczeń:
- Orzeczenie o niepełnosprawności – najczęstsze, uprawniające do zasiłku i ulg podatkowych
- Orzeczenie o niepełnosprawności ze wskazaniem konieczności stałej lub długotrwałej opieki – dla pacjentów z ciężką niepełnosprawności
- Orzeczenie o niepełnosprawności ze wskazaniem konieczności pobytu w domu opieki – dla pacjentów wymagających 24-godzinnej opieki
Procedura uzyskania orzeczenia obejmuje złożenie wniosku w Powiatowym Zespole ds. Orzekania o Niepełnosprawności (PZON), przygotowanie dokumentacji medycznej i przejście badania przez komisję lekarską.
Świadczenia i zasiłki
Pacjenci ze spastycznością mogą kwalifikować się do różnych świadczeń:
- Zasiłek z tytułu niepełnosprawności – miesięczne świadczenie pieniężne
- Świadczenie pielęgnacyjne – dla opiekunów pacjentów wymagających codziennej opieki
- Zasiłek opiekuńczy – czasowe wsparcie
- Renta z tytułu niezdolności do pracy – dla dorosłych pacjentów niemogących pracować
PFRON – Państwowy Fundusz Rehabilitacji Osób Niepełnosprawnych
PFRON udziela dofinansowania na zakup sprzętu ortopedycznego i rehabilitacyjnego. Pacjenci ze spastycznością mogą kwalifikować się do dofinansowania na: ortezy, szyny, wózki inwalidzkie, pionizatory, sprzęt rehabilitacyjny.
Procedura ubiegania się o dofinansowanie PFRON obejmuje przygotowanie wniosku, zaświadczenia od lekarza oraz wyceny sprzętu. Kwoty dofinansowania są ograniczone, ale mogą pokryć znaczną część kosztów.
Turnusy i pobyty rehabilitacyjne
Turnusy rehabilitacyjne to intensywne pobyty terapeutyczne, zwykle 3-4 tygodnie, w specjalistycznych ośrodkach. Turnusy mogą być finansowane przez NFZ dla pacjentów spełniających określone kryteria.
Turnusy oferują intensywną terapię ruchową, zajęciową, logopedyczną oraz wsparcie psychologiczne. Pobyty mogą być szczególnie przydatne dla pacjentów w fazie ostrze (np. w pierwszych miesiącach po udarze).
Wsparcie psychologiczne
Spastyczność może powodować znaczące emocjonalne wyzwania dla pacjentów i ich rodzin. Depresja, niepokój, frustracja i brak pewności siebie są częstymi konsekwencjami.
Wsparcie psychologiczne może obejmować:
- Terapia indywidualna – rozmowy z psychologiem lub psychoterapeutą
- Terapia grupowa – spotkania z innymi pacjentami ze spastycznością
- Wsparcie rodzinne – porady dla rodzin na temat opieki i zarządzania zaburzeniami
- Edukacja pacjenta – informowanie pacjenta o spastyczności, dostępnych leczeniach i strategiach samoopieki
Wsparcie psychologiczne powinno być częścią kompleksowego podejścia do leczenia spastyczności.
Edukacja i informacja
Edukacja pacjenta i rodziny jest kluczowa do sukcesu leczenia. Pacjenci, którzy rozumieją spastyczność, dostępne opcje leczenia i mogą aktywnie uczestniczyć w swoim leczeniu, osiągają lepsze wyniki.
Edukacja powinna obejmować:
- Wyjaśnienie przyczyn spastyczności
- Opisanie dostępnych opcji leczenia
- Instrukcje dotyczące ćwiczeń domowych i pozycjonowania
- Informacje o możliwościach wsparcia społecznego
- Porady dotyczące przystosowania do spastyczności
Pacjenci mogą otrzymywać edukację od lekarzy, fizjoterapeutów, terapeutów zajęciowych oraz poprzez материалы edukacyjne i zasoby online.
Jak samodzielnie zarządzać spastycznością w domu
Pacjenci mogą wykonywać wiele działań w domu, aby zmniejszyć spastyczność i poprawić funkcjonowanie:
Ćwiczenia domowe
Ćwiczenia domowe są kluczowe do utrzymania postępów osiąganych w terapii zawodowej. Terapeuta powinien nauczyć pacjenta lub opiekuna, jak wykonywać ćwiczenia, a pacjent powinien je praktykować codziennie.
Ćwiczenia domowe mogą obejmować:
- Rozciąganie mięśni – powolne, łagodne rozciąganie mięśni przez 30-60 sekund, powtarzane kilka razy
- Wzmacnianie mięśni – ćwiczenia przeciwko oporowi
- Ćwiczenia równoważące – dla pacjentów, którzy mogą stać
- Ćwiczenia funkcjonalne – praktyka codziennych czynności
Konsystencja jest klucz – ćwiczenia domowe powinny być wykonywane każdego dnia, a nawet kilka razy dziennie dla najlepszych wyników.
Pozycjonowanie w domu
Pacjenci mogą stosować pozycjonowanie w domu poprzez:
- Używanie szyn na noc
- Regularną zmianę pozycji
- Podpieranie mięśni pod prawidłowymi kątami
- Używanie poduszek do wsparcia
Opiekun powinien być poinstruowany, jak prawidłowo umieścić pacjenta w pozycji, która zmniejsza spastyczność.
Ciepło i relaksacja
Ciepła woda lub ciepłe okłady mogą zmniejszyć spastyczność poprzez relaksację mięśni. Pacjent może wziąć ciepłą kąpiel lub przyłożyć grzejnik do spastycznych mięśni przed ćwiczeniami.
Relaksacyjne techniki oddychania i medytacji mogą również zmniejszyć spastyczność poprzez zmniejszenie napięcia psychicznego.
Natomiast monitorowanie i utrzymanie komunikacji z zespołem
Pacjent powinien regularnie informować swojego lekarza o zmianach spastyczności, efektywności leczenia i nowych problemów. Regularne wizyty (co 4-12 tygodni w zależności od stabilności) pozwalają na dostosowanie leczenia.
Pacjent powinien prowadzić dziennik spastyczności, zanotowując nasilenie objawów, czynniki, które pogorszają lub poprawiają spastyczność, oraz efekty uboczne leków.
Podsumowanie
Spastyczność to złożony problem neurologiczny, który wymaga wielowymiarowego podejścia do leczenia. Farmakoterapia, rehabilitacja, wsparcie psychologiczne i społeczne, oraz samoopieka pacjenta są wszystkie ważne dla osiągnięcia optymalnych wyników.
Pacjenci ze spastycznością mogą osiągnąć znaczną poprawę funkcjonowania poprzez:
- Wczesną diagnozę i interwencję
- Kompleksowe leczenie farmakologiczne (baklofen, tizanidyna, toksyna botulinowa)
- Intensywną fizjoterapię (NDT-Bobath, Vojta, PNF)
- Pozycjonowanie i rozciąganie mięśni
- Zaopatrzenie ortopedyczne (ortezy, szyny, wózki)
- Wsparcie społeczne i psychologiczne
- Edukację i samoopieka
W Polsce pacjenci mogą korzystać z comprehensive care dostępnego poprzez NFZ, ośrodki rehabilitacyjne specjalistyczne, oraz prywatne usługi. Kluczem jest aktywne zaangażowanie pacjenta i rodziny w proces leczenia.
Meta opis: Spastyczność to wzmożone napięcie mięśniowe wymagające leczenia farmakologicznego, fizjoterapii i wsparcia. Kompletny przewodnik przyczyn, terapii, rehabilitacji i opieki dla pacjentów w Polsce.

Pisze artykuły o zdrowiu ze swojego punktu widzenia